每年2月份的最后一天是国际罕见病日。罕见病是指那些发病率极低的疾病,博鳌亚洲论坛2025年年会期间,北京协和医院院长、党委副书记、中国医学科学院北京协和医学院副院校长张抒扬介绍,有7000多种或者上万种的罕见病,目前仅仅有5%的罕见疾病有有效的药物治疗。
今天,我们跟随海口市人民医院肾病风湿科主治医师雷文娟了解一种名为“非典型溶血性尿毒症综合征(aHUS)”的罕见病。
生死48小时
今年34岁的患者刘女士不久前因"腹痛2天"急诊入院。“起初家属误以为是痛经,但随后患者出现少尿、呼吸困难等症状。”雷文娟介绍,经过实验室检查,结果显示:血红蛋白下降至47g/L(正常115-150),血小板最低降至34×10⁹/L(正常100-300),血肌酐飙升至941μmol/L(该患者正常值41-73)。
在短短48小时内,患者病情迅速发展,危及生命。海口市人民医院肾病风湿科医疗团队结合临床经验,初诊刘女士患的是血栓性微血管疾病,立即启动血浆置换,后续结合补体相关检查,最终诊断为非典型溶血性尿毒症综合征(aHUS),并给予补体抑制治疗。经过系统治疗,患者病情得到缓解,肾功能恢复正常,并重返职场,备孕二胎。
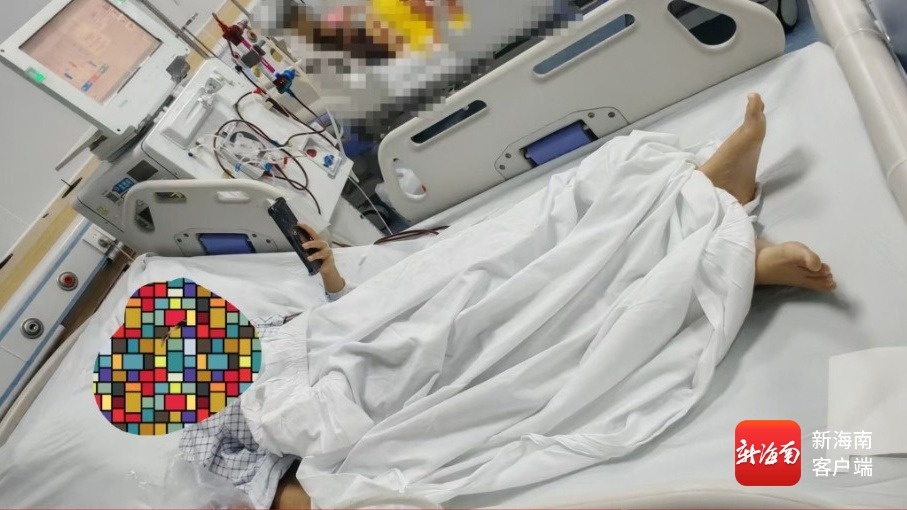
患者在接受治疗。受访者供图
雷文娟介绍,aHUS是一种罕见的、威胁生命的血栓性微血管病,发病率约百万分之七,在2018年已被纳入我国《第一批罕见病目录》。其核心特征是微血管内血小板异常聚集,导致溶血性贫血、血小板减少和急性肾损伤三联征。补体系统是人体免疫防御的一部分,如同体内的“巡逻兵”。在aHUS患者中,由于先天遗传或后天获得性原因,这个系统出现了“bug”,导致补体旁路途径被不可抑制地持续激活。
她介绍,该病没有地域差异,近两年该院治疗过五六例患者。
病因复杂,主要有3类
雷文娟介绍,aHUS的致病因素比较复杂,主要有3类。一是遗传因素:多数患者存在补体相关因子的基因突变,如补体因子H(CFH)、CD46、补体因子I(CFI)、C3等。这些突变使得调节补体活化的“刹车”失灵。二是获得性因素:约6%-10%的患者体内产生了针对补体因子(如H因子)的自身抗体,同样导致补体系统过度活化。三是诱发因素:感染、妊娠、自身免疫疾病、某些药物等是常见的“触发器”,可在具有遗传易感性的个体中激发疾病。
失控的补体系统最终形成膜攻击复合物,损伤血管内皮细胞,引发微血栓形成。这直接导致了红细胞在通过狭窄的病变血管时被机械性破坏(溶血),血小板被大量消耗,以及肾脏等重要器官因缺血而功能衰竭。
aHUS可发生于各年龄段,常急性起病,病情进展迅速,在临床表现与诊断上,识别“三联征”是关键。其典型症状有:贫血表现,如面色苍白、乏力、精神萎靡;肾脏受损表现,如尿色加深如浓茶色或酱油色、尿量减少甚至无尿、水肿、血压升高;出血倾向,如因血小板减少,但皮肤紫癜等明显出血相对少见;部分患者可出现神经系统症状(如头痛、视物模糊、惊厥)、胃肠道症状(腹痛、呕吐)等。
其诊断主要依靠临床表现和实验室检查。如:微血管病性溶血性贫血,血红蛋白显著降低(常低于80-100g/L),外周血涂片可见破碎红细胞,乳酸脱氢酶(LDH)升高,而Coombs试验阴性;血小板减少,血小板计数下降(通常低于150×10⁹/L);急性肾损伤,血肌酐进行性升高,常伴有血尿、蛋白尿。同时,需要排除典型腹泻后HUS、血栓性血板减少性紫癜(TTP)等其他疾病。补体C3水平降低、检测到相关基因突变或自身抗体,可进一步支持诊断。
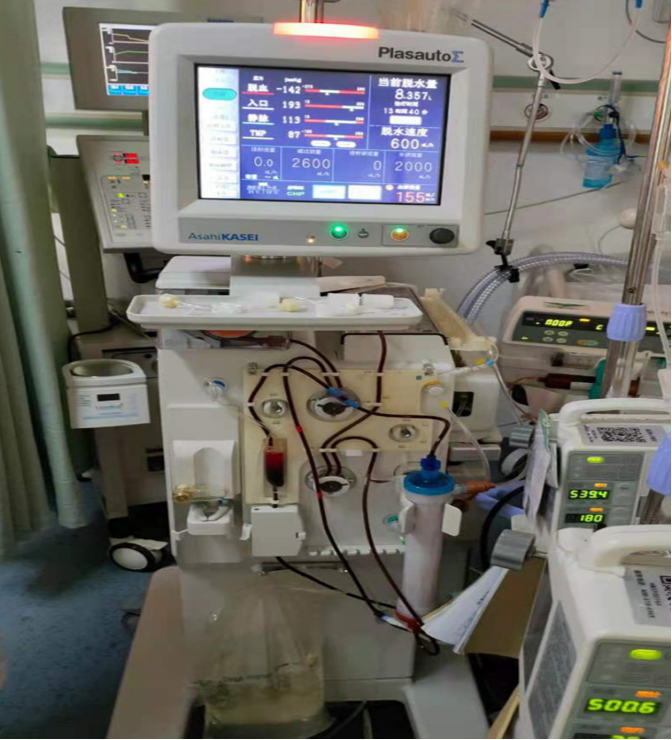
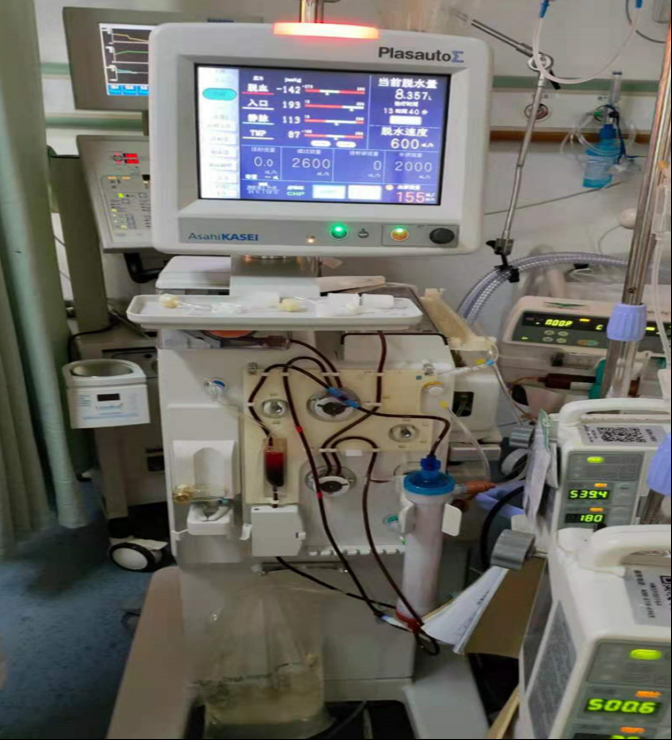
血液净化治疗仪器。受访者供图
从传统疗法到靶向突破
雷文娟表示,aHUS预后差,急性期死亡率曾高达20%-25%,且近半数患者可能进展为终末期肾病(尿毒症)。因此,早期诊断、及时规范治疗至关重要。
在传统治疗方面,有血浆疗法:包括血浆置换或新鲜冰冻血浆输注,曾是标准一线治疗。但约半数患者反应不佳,尤其对遗传性aHUS疗效有限。支持治疗:包括纠正贫血(输注红细胞)、控制出血风险、营养支持、控制血压,以及必要时进行透析治疗。
在靶向治疗方面,采取补体抑制剂。近年来,补体C5抑制剂(如依库珠单抗)的应用是aHUS治疗领域的革命性突破。它能精准阻断过度活化的补体终末途径,从源头抑制血管内皮损伤和血栓形成。早期使用可以大大改善预后,更好地保护肾脏功能,降低死亡率和复发风险。
此外,对于抗H因子抗体阳性的患者,可联合使用激素和免疫抑制剂。对于已发展为终末期肾病的患者,肾移植是一种选择,但移植肾存在复发的风险。
雷文娟表示,由于aHUS有复发风险,患者需要长期随访管理。要定期复查血常规、肾功能、尿常规等指标,密切关注尿量、尿色变化。避免劳累、预防感染、保持情绪稳定。饮食上需根据肾功能情况,在医生指导下控制蛋白质、盐、钾、磷的摄入,并保证充足热量。有家族史的人群可进行遗传咨询,对于高风险个体,应尽量避免感染、妊娠等诱发因素的影响。